今回より、「簡易型センサー技術」に関する最近の報告(Anal. Chem.)から幾つか、概略を紹介します。
<前置き>
・簡易検査/POCT(Point of care testing)はもともとベッドサイドや手術時などの緊急検査として開発され、簡易型デバイス技術をベースとしています。POCT検査キットは迅速で簡便な検査法であるために、国内では一般的な臨床検査にも使われており定着してきています。このPOCT技術は欧米ではラテラルフローイムノアッセイ(LFA;Lateral Flow assays/Lateral Flow Immunoassays)として周知されています。日本ではイムノクロマトグラフィーアッセイ(Immuno-Chromatography Assay)、或はストリップテスト(Strip test)としても知られています。
このLFAは洗練された技術として開発され、既に1960年代に基礎技術が報告されており、誰でも簡単に取り扱いの出来る便利な検査手法です。一般的に普及したLFA検査としては妊娠検査薬などがあり、臨床検査は言うに及ばず、獣医学、農学、食品産業、生体防御や環境など幅広い分野で多く利用されています。
◆簡易型デバイスの検査キット;
・2010年までに世界で100社以上がLFA製品を生産しており、その市場規模は約3,360億円*1(1$=100円換算)にもなっており、コスト効果、ポータブル、測定の簡便性及び迅速性などの点で、LFA法は、既存のELISAやPCR法などより優れています。
・通常、ELISAではプラスチックウエルを固相に用いていますが、LFA法ではニトロセルロース膜を固相としており、測定対象をトラップする抗体または抗原を固定化しています。ELISA等の操作が複数ステップなのに比べて、この膜を利用したデバイス型LFA検査法は1ステップ測定が可能であることに特徴があります。
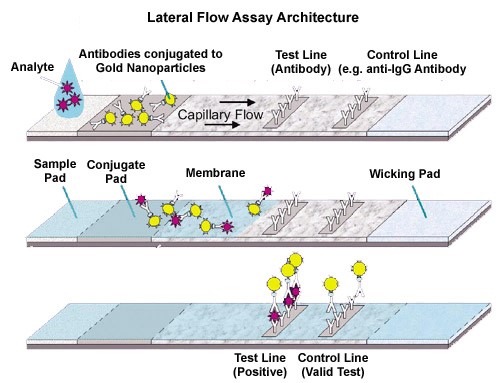
・典型的なLFAデバイスを図1に示します。その基本的な構成要素は、1;サンプルパッド、2;コンジュゲートパッド、3;ニトロセルロース膜、4;吸収パッドの4つのセグメントからできており、その各機能も付記しました。
*1;Anal.Chem.;88,6441–6449, 2016.
1、サンプルパッド(Sample pad)→ 検体サンプルを点着する吸着パッド
2、コンジュゲートパッド(Conjugate pad) 、または 試薬パッド(reagent pad)→ 標識体; 特異的抗体を結合した着色ラッテクス微粒子(又は金コロイド粒子など)、主にニトロセルロース膜使用。
3、反応メンブレン(Reaction membrane)→ 測定対象と反応する抗体をライン状に固定化(テストライン)
4、吸水リザーバー、または廃液リザーバ(Wick or waste reservoir)→ 毛管現象(Capillary force)によって、反応膜へ移動したサンプルを吸い上げる吸収パッド。
―[簡易型デバイスによるLFAの測定技術‐1]―
◆簡易型デバイスによるAFI関連ウイルスに対する、感染初期におけるIgGおよびIgM抗体の同時測定;
・論文;Anal.Chem.;88、8359–8363、August 4, 2016 (Letter)
DOI:10.1021/acs.analchem.6b01828
・著者;Seoho Lee, et.al.,
・所属;コーネル大(NY、Ithaca)機械工学・大気圏工学
・タイトル;Two-Color Lateral Flow Assay for Multiplex Detection of Causative Agents Behind Acute Febrile Illnesses
・デング熱やチャングニア熱など症状が類似している急性未分化熱病疾患(AFIS; Acute undifferentiated febrile illnesses)は、デングウイルス(DENV)、チャングニア熱ウイルス(CHIK)などによって引き起こされる感染症であり、その鑑別診断は患者を適切にマネジメントするためにクリティカルであって、感染初期に検出することが重要となります。
・ウイルスに対するIgG抗体およびIgM抗体の検出は、幾つかの熱病疾患を鑑別するために使われておりますが、ここに挙げたAFI関連ウイルスを同時に、かつ簡便で迅速なアッセイが可能でとなる簡易型デバイスのPOCT検査キットによる測定が望まれております。従って、単一のウイルス病原体(抗原)に対するIgGおよびIgM抗体を同時に検出できる迅速診断テスト(RDT;Rapid Diagnostic test)は、急速診断が必要な際に重要な役割を果たすことができます。
・本論文は、2種類のカラーラテックス粒子を検出に用いて、単一ストリップ型デバイスによる複数のウイルス抗体*2を同時に検出できる新たなLFAを報告しております。そのLFAデバイスの構成要素を図2に示します。
*2;ウイルス2種のIgGならびにIgM抗体、計4種類の抗体
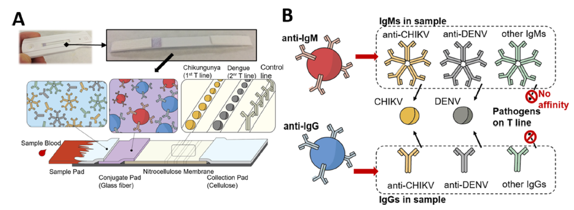
図2、IgGおよびIgMを同時検出するLFA法の構成要素;
A;アッセイデバイス;サンプルパッド、コンジュゲートパッド、ニトロセルロース膜(テストラインおよびバリデーションライン)と、回収パッドの4つの構成要素からなっている。
*テストラインにはウイルス2種類のリコンビナント抗原を固定化;リコンビナントCHIKVのE2抗原、リコンビナントDENVのdengue antigen。
B;アッセイ成分;青ラテックス粒子(抗IgG抗体感作;抗ウイルスIgGと結合)、赤ラテックス粒子(抗IgM抗体感作;抗ウイルスIgMと結合)。
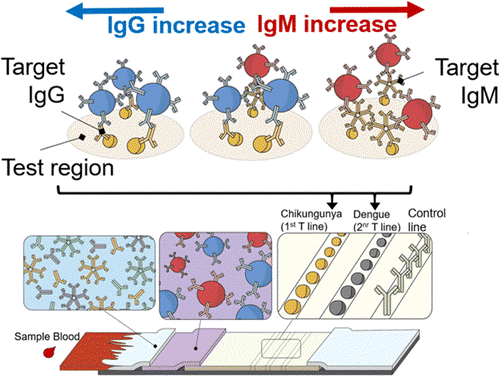
・このLFAでは、迅速にIgG/IgMを多重検出できるようにするために、標識体として青と赤の2種類のカラーラテックス粒子を用いた新たなアッセイ系を提示しています(図3)。テストラインは2つあり、1つはデングウイルス(DENV)、もう一つはチャングニア熱ウイルス(CHIK)に対するラインで、ラインには各ウイルスのリコンビナント抗原が固定化されています(図2)。サンプル中の抗体と反応し、移動してきた抗体結合カラーラテックス粒子は、このライン上で、結合し、捕獲されてシグナルとなります。テストラインで捕獲されなかった過剰なカラー粒子はさらにコントロールライン上で捕獲・結合されてテストの有効性を示すバリデーションとなります。
アッセイ系;サンプルパッド層に血液(血漿/血清)を点着し、コンジュゲートパッド層内の青ラテックス粒子および赤ラテックス粒子は、サンプル層から移動した抗ウイルスIgG或はIgM抗体と反応して結合し、各抗体結合カラー粒子は移動して、ニトロセルロース膜上のテストライン層で、ウイルスのリコンビナント抗原と結合する。
*デバイス上でのサンプルなどの移動の流れは毛細管現象。
・図3のアッセイスキームによって、DENVおよびCHIKVに対する4種類のIgGおよびIgM抗体が10分以内に検出可能となります(図4)IgG、IgG/IgM、及びIgM陽性、それぞれのケースに対応して、ブルー(B)、ミックス(G)、及びレッド(R)のカロリメトリックのシグナルが、明瞭な色調強度イメージを伴って検出され、正確な12種の異なる診断シナリオにすることができます。
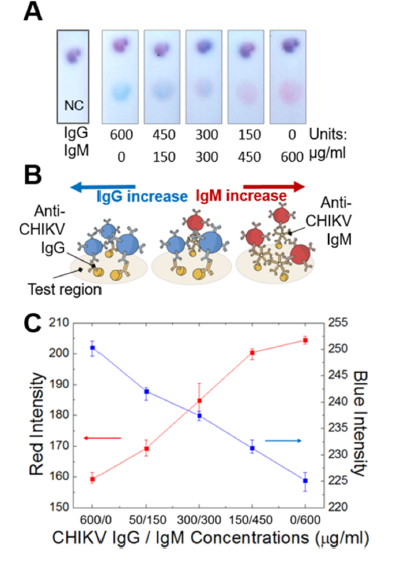
CHIKVに対する2種類の IgGおよびIgM抗体の検出;
A;2カラーアッセイのテスト領域におけるカラー展開したシグナルスポット。IgG抗体600から0Units、対応するIgM抗体は0から600μg/mLの組み合わせ。
B;抗CHIKVの IgG及びIgM抗体を結合させたブルー粒子とレッド粒子とのテストライン領域上での相互作用の模式図。
C;テストライン領域でのブルーとレッドシグナル強度のイメージ分析;縦軸は光強度、横軸は抗CHIKVのIgG/IgM抗体の組み合わせ濃度。
・シグナル検出: iPhone(8メガPixel CMOSカメラ/5秒)
・サンプル量;10μL、展開緩衝液;80μL
・測定時間(LF);10分間
・各種の臨床サンプルによるLFAによる検討結果を図5に示します。テストライン上に、青から赤までの色調変化が読み取れています。これらの色はR,G,Dの3種類のカラーの組み合わせで出来ており、IgG、IgG/IgMおよびIgMが少なくとも、それぞれ3区分(Hue値;200-209、227-247、262-290)の範囲で識別できます。
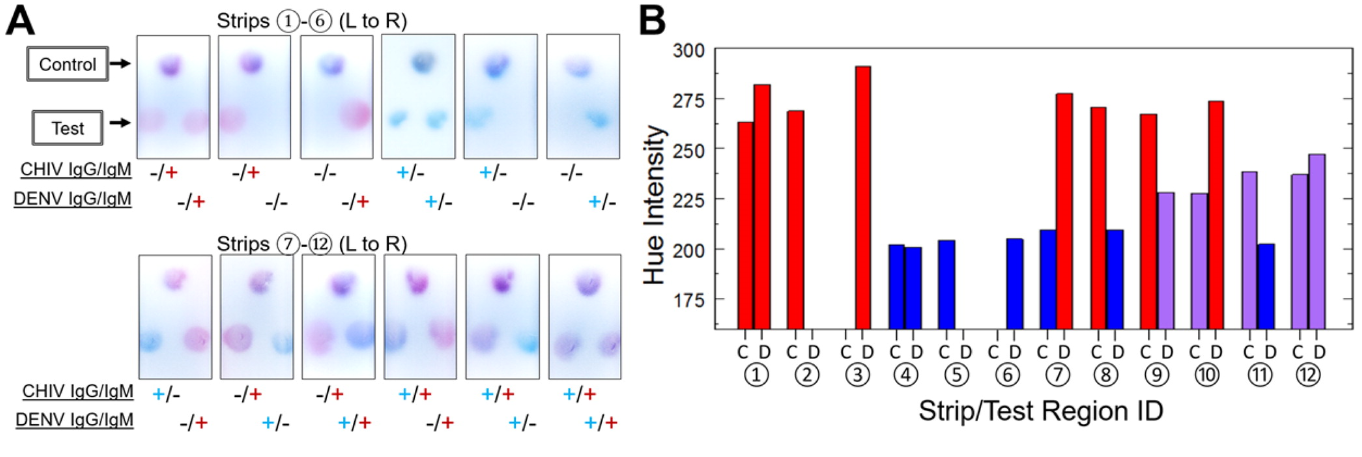 図5;シングルストリップ上でのCHIKVとDENVのIgG/IgMテスト;
図5;シングルストリップ上でのCHIKVとDENVのIgG/IgMテスト;
A; 下段スポット、左;CHIKV(C)、右;DENV(D)のテスト領域の色調。上段;テストバリデーションのコントロール
B;テスト領域でのCHIKVとDENVの色合いのHue強度(R,G,B組み合わせ強度;数式で得られる平均値)。
①~⑫;臨床サンプルの番号
・このLFAはスマートホン使用による解析ができるので、POCT検査としての要件を満たしています。この技術は、将来、正確性と自動診断をなすための分析システムとして、偉業となるかもしれません。これは対象となる多くのAFISの鑑別診断のための、単一RDTをベースとしたシステム開発に対する第1歩になる可能性があります。