<最近の検査法1>
これまで紹介してきました「検査技術の発展」を一旦、お休みして、最近の論文から検査領域におけるバイオマーカー関連技術動向の一端を紹介したいと思います。
リボ核酸RNAにはタンパク質合成の翻訳を担うmRNA、ノンコーディングRNAのtRNAやrRNAがあります。さらにRNA干渉*1 で一躍、脚光を浴びた短鎖のsiRNAが知られています。この外に、一本鎖の短いRNAとしてマイクロRNA(miRNA)があります。このmiRNAは遺伝子の転写後調節に極めて重要な役割を果たす因子として注目されています。
一方、疾患やウイルス感染などでもmiRNAは重要な働きをしているようで、がん型・ステージなどで特異的な発現をしており、新規のバイオマーカーや予後マーカー候補としても期待されております。また細胞外に分泌されるエクソソーム(exosome)中にもmiRNAが存在し、最近、エクソソーム(グリピカン1)が膵臓がんマーカーになるかもしれいとの報告*2もあり、また、国立がんセンターを中心としたmiRNA測定技術基盤の研究開発*3では、患者の分泌型miRNAを網羅的に解析して、新たながんマーカー診断法の確立を目指しており、13種のがん(胃、食道、肺、肝臓、胆道、膵臓、大腸、卵巣、前立腺、膀胱、乳、肉腫、神経膠)が1滴の血液で測れるとのことで話題を呼んでおります。
そこで、今回はmiRNAに関する最近のClin.Chem.に報告された幾つかの話題を紹介したいと思います。
(1)自動イムノアッセイ装置によるアルツハイマー病(AD)に関連するmiRNAの測定についてドイツ・シーメンス社の報告*4:Kappel & Keller(Siemens AG);「Automation and Analytical Techniques;MicroRNA In Vitro Diagnostics Using Immunoassay Analyzers.Clin.Chem.,61:4,600-607,2015.
・現在、使用されているmiRNA検出法;定量的RT-PCR(qRT-PCR)、マイクロアレイや次世代シークエンサー(NGS)が比較的高コストで、操作が煩雑であること、市販されているqRT-PCRプラットフォームが組織向けであることなど、ルーチン使用にはまだ改善の余地がありそうです。本論文では、臨床検査ラボにある既存の自動装置ACIS(Advia Centaur Immunoassay System)によってmiRNAが測定できる新しい方法を開発している。その方法は、血中miRNAを増幅することなく、miRNAに相補的なDNAとヘテロハイブリダイズさせて捕獲し、このDNA/RNAヘテロポリマーに対する標識モノクローナル抗体を用いた新しいイッムノアッセイです。このイムノアッセイプロセスを自動化させ、ACIS装置によってアッセイシステムの性能を検討し、AD病患者血清miRNAを評価している。このDNA/RNAヘテロポリマーに対するモノクローナル抗体を利用する方法は、1986年にボガロスキーらによって初めて報告*5されたものです。
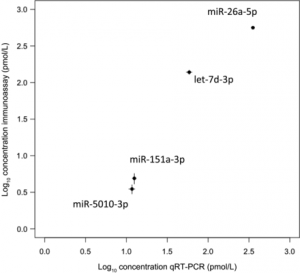
・このACIS装置による測定の結果、miRNAの測定範囲は1 pmol/Lから1 nmol/Lで、特異性(Analytical specificity)は99.4%、測定感度(Lower limit of Detection)は1 pmol/Lであった。 ヒト血液サンプルによる4種のADパネルmiRNAs(miR-26a-5p,let-7d-3p,miR-151a-3p,miR-5010-3p)の測定では、82%の診断精度でAD病を検出できるようであり、既存のqRT-PCR法と0.994の高い相関性を示している(図1)。
・このACIS装置による新自動アッセイ法は、増幅プロセスが不要で、かつ高い再現性があり、分析結果は3時間以内に得られということで、短時間、低コストでのハイスループットが可能なmiRNAの自動測定が実用化できると述べられている。また、8項目の同時アッセイ(多項目1検体中)も可能であるが、感度面で若干低下し、今後の課題となっている。
・血中には分泌型miRNAを含め、多くのmiRNAがあり、今後、疾患との関連で検査ターゲットとなりうるバイオマーカーとして、miRNAの自動測定による臨床展開が期待される。
図1、アルツハイマー病血液サンプルmiRNAのqRT-PCRとの相関*4
===================================
*1;Fire, et.al., Potent and specific genetic interference by double-stranded RNA in Caenorhabditis elegans.Nature 391, 806-811, 1998.(2006年ファイアはRNAiの発見によりノーベル生理学・医学賞)
*2;SA. Melo, et.al., Glypican-1 identifies cancer exosomes and detects early pancreatic cancer. Nature 523, 177–182.2015.
*3;http://www.ncc.go.jp/jp/information/press_release_20140818.html
*4;Kappel & Keller(Siemens AG);「Automation and Analytical Techniques;MicroRNA In Vitro Diagnostics Using Immunoassay Analyzers.Clin.Chem.,61:4,600-607,2015.
*5;Boguslawski,et.al.;Characterization of monoclonal antibody to DNA.RNA and its application to immunodetection of hybrids. J Immunol Methods. 89(1):123–130, 1986.
(技術の補足)本論文の測定法;
・測定システムは4ステップからなるサンドイッチイムノアッセイ法であって、全自動測定システム(Advia Centaur Immunoassay System/Siemens Healthcare Diagnostics)を用いている。
・反応の基本系は、固相系に捕獲用のDNAで標的となるシングルmiRNAに相補的な配列をもつビオチン化オリゴヌクレオチド、サンプルmiRNAを結合したオリゴヌクレオチドを、ビオチンとSAを介して粒子に結合させるためのSA結合マイクロ粒子から構成されている。
・標識抗体系はアクリジニウムエステルを標識した、DNA/RNAヘテロハイブリッドに特異的に結合するモノクローナル抗体。
・検出系は、酸、またはアルカリを添加することでアクリジニウムからの化学発光を測定する。
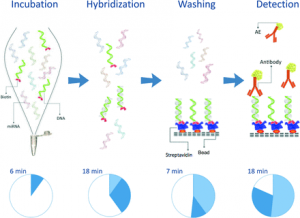
・反応の概要(図2);まず血液から精製したmiRNAをオリゴDNAと6分間混合し、引き続いて18分間ハイブリダイゼーションをする。次にこの混合水溶液をストレプトアビジン(SA)固定化粒子に加えて7分間インキュベートした後、ハイブリダイズしたmiRNAが固相のSAにトラップされる。 洗浄後、AE標識モノクローナル抗体を加え、酸/アルカリを添加することで生じるアクリジニウムからの化学発光を18分間計測する。反応時間は、計49分となる。
図2、完全自動化イムノアッセイによる主要な反応ステップ;AE;アクリジ二ウムエステル、灰色DNA;miRNA、緑色DNA;ビオチン化オリゴDNA(赤;ビオチン)。青色;ストレプトアビジン(SA)固定化粒子。抗体;AE標識モノクローナル抗体(のDNA/RNAヘテロハイブリッドに特異的に結合)*4http://www.clinchem.org/content/61/4/600.full
(2)miRNAs発現プロファイルにもとづいた早期乳がんを検出するための循環中miRNAs同定についての報告;Matamala,et.al.;(Spanish National Cancer Research Centre);Tumor MicroRNA Expression Profiling Identifies Circulating MicroRNAs for Early Breast Cancer Detection. Clin. Chem.; 61, 1098-1106. 2015.
・乳がん患者の血漿中miRNAsが、乳がんの早期検出に利用できる可能性を示唆している。患者83例(治療前36例、治療後47例)、健常人26例の血漿サンプルを分析し、114例の治療前患者と116例の健常者サンプルで評価、検証している。
・乳がん患者のヒト組織(パラフィン包埋組織1919個、健常組織サンプル11例)からmiRNAs発現プロファイルを調べ、多数同定し、高い感度と特異性で腫瘍を識別できるmiRNAs25種を開発した。このmiRNAsから10種選び、さらに4種 miR-505-5p, miR-125b-5p, miR-21-5p, and miR-96-5pが、健常者血漿と比較して有意に過剰発現していた。MiR-505-5p及び miR-96-5pは最も価値のあるバイオマーカー(ROC曲線0.72)であったと結論づけており、さらにmiR-3656, miR-505-5p及びmiR-21-5pの発現レベルは治療患者では低下していた。
(3)miRNA標準化の動き;測定手法の違いによるmiRNA濃度の差異について標準化検討の報告(レビュー);Schwarzenbach(University Cancer Center Hamburg),da Silva(The University of Texas MD Anderson Cancer Center),Calin(Universidade do Porto,);Data Normalization Strategies for MicroRNA Quantification. Clin. Chem. 61, 1333-1342. 2015.
miRNAの発現レベルの測定法(qT-PCR、マイクロアレイ法)の開発におけるmiRNA定量化には、内在性や外部比較遺伝子を用いた標準化がなされてきているが、標準化戦略のコンセンサスはない。比較遺伝子の選択が問題視されており、実際の転写物に影響し、データ解釈に問題が生じている。 このレビューでは、miRNAを用いる信頼性、グローバル標準法の確立について議論している。
(4)循環中miRNAのがんバイオマーカーとしての現状(レビュー);He,et.al.;Guangdong Medical University,China);Current State of Circulating MicroRNAs as Cancer Biomarkers;Clin. Chem.61,1138-1155, 2015.